Propiedades Químicas
Los éteres tienen muy poca reactividad química, la desaparición del enlace C - H de los alcoholes reduce considerablemente el comportamiento químico de los éteres y solamente se presenta el que corresponde al enlace C - O. El enlace C-O es fuerte, lo que explica, la baja reactividad de estas sustancias. esta propiedad les confiere una buena capacidad disolvente. sin embargo, algunos éteres reaccionan lentamente con el aire para formar peróxidos, compuestos que contienen enlaces O-O.
REACCIÓN CON LOS HALUROS DE HIDRÓGENO:
Los haluros de hidrógeno son capaces de romper los enlaces del oxigeno del éter y formar dos moléculas independientes. Los éteres alifáticos se rompen en dos moléculas del haluro del alquílo correspondiente, mientras que en los éteres alquilo se forman el alquilo haluro correspondiente y fenol. Las reacciones que siguen con el HI sirven para ilustrar.
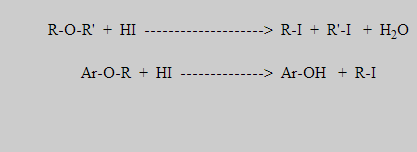
REACCIÓN CON EL OXIGENO DEL AIRE:
Cuando los éteres están en contacto con el aire, espontánea y lentamente se produce su oxidación que genera un peróxido derivado muy inestable. la presencia de estos son un elevado peligro potencial cuando el éter se somete a un proceso de destilación. en este caso, los peróxidos en el liquido no destilado aun, se van concentrando y pueden producir una violenta explosión.
Los ésteres presentan el efecto inductivo:
HIDROLISIS ESTEÁRICA:
La ruptura de un éster por agua se denomina la hidrólisis esteárica. También pueden ser descompuestos por ácidos o bases fuertes. Como resultado, se descomponen en un alcohol y un ácido carboxilico, o una sal de un ácido carboxilico.
HIDRÓLISIS ÁCIDA:
Por calentamiento con agua se descompone en el alcohol y el ácido de los que proviene.
éster + agua ----------- ácido + alcohol
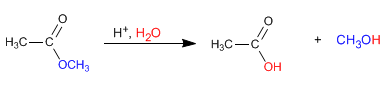
Con un exceso de agua la reacción es total. Es un proceso inverso a la esterificación.